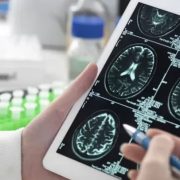
Estados Unidos aprobó un medicamento que retrasa el avance del Alzheimer
La Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) concedió el martes la aprobación a un fármaco contra el Alzheimer muy vigilado, concluyendo que los beneficios de ralentizar modestamente la progresión de la devastadora enfermedad superan sus riesgos, anunció la farmacéutica Eli Lilly.
El donanemab, comercializado bajo la marca Kisunla por la farmacéutica Eli Lilly, es la segunda droga que demostró de manera convincente un retraso en el deterioro cognitivo. En diciembre pasado la FDA había aprobado la droga Leqembi, de la empresa japones Eisai.
Ambas drogas tienen un funcionamiento similar. Se aplican como infusiones intravenosas y tiene como objetivo atacar la proteína involucrada en el desarrollo de la enfermedad. El desarrollo de Eli Lilly se aplica una vez al mes, mientras que la del laboratorio Eisai se administra cada dos semanas, informó The New York Times. Otra diferencia es que la nueva droga puede dejar de aplicarse cuando se eliminó la placa de la proteína amiloide en el cerebro.
Las autoridades indicaron que Kisunla está destinado a pacientes en una etapa temprana de Alzheimer. Además, añadieron que las demoras de los efectos cognitivos se difiere en unos meses, hasta siete en el caso del donanemab.
Los pacientes y sus familias tendrán que sopesar ese beneficio frente a las desventajas, incluidas las infusiones intravenosas periódicas y los efectos secundarios potencialmente peligrosos, como la inflamación y el sangrado cerebral, indicó la agencia AP.
Los especialistas, sin embargo, destacan que los resultados son un paso adelante en el tratamiento en personas con Alzheimer. «Estoy encantada de tener diferentes opciones para ayudar a mis pacientes. Ha sido difícil como especialista en demencia: diagnostico a mis pacientes con Alzheimer y cada año veo que empeoran y el cuadro avanza hasta que mueren», expresó Suzanne Schindler, neuróloga de la Universidad de Washington en St. Louis.
Un pionero polémico para tratar el Alzheimer
En rigor, los productos Leqembi y Kisunla no son los primeros experimentos aprobados por la FDA para tratar la enfermedad de Alzheimer. En junio de 2021 el organismo estadounidense aprobó otro medicamento que prometía avances inéditos en dos décadas de investigación. Se llamaba Aduhelm y su lanzamiento estuvo envuelto en polémica. A comienzos de 2024 dejó de comercializarse.
«Aduhelm es el primer tratamiento dirigido a la fisiopatología subyacente de la enfermedad de Alzheimer, la presencia de placas de beta amiloide en el cerebro», aseguró Patrizia Cavazzoni, de la FDA. Era junio de 2021. La ilusión era concretar avances en el tratamiento farmacológico contra el Alzheimer. Buscaban atacar el proceso desencadenante de la demencia, en lugar de solo tratar sus síntomas.
La «aprobación acelerada» produjo una fuerte polémica en Estados Unidos, donde los especialistas advirtieron sobre la debilidad de los resultados de los ensayos en humanos.
Hubo dos pruebas: una mostró una reducción en el deterioro cognitivo; la otra, no.
Sin embargo, en ambos estudios demostró de manera convincente una reducción en la acumulación de una proteína llamada beta-amiloide en el tejido cerebral de los pacientes con Alzheimer.
Una teoría sostiene que la enfermedad de Alzheimer se produce por una acumulación excesiva de estas proteínas en el cerebro de algunas personas a medida que envejecen y su sistema inmunológico se deteriora.
Por lo tanto, proporcionar anticuerpos a estos pacientes podría ser un medio para restaurar parte de su capacidad para eliminar la acumulación de placa.
Finalmente, en enero pasado, la empresa farmacéutica Biogen abandonó los derechos de propiedad del aducanumab, la sustancia que se vendía bajo el nombre comercial de Aduhelm. Fue un estrepitoso fracaso de mercado y también fue considerado un fallo para el sector farmacéutico. La empresa continuaba, aun tres años después de su lanzamiento, con análisis para verificar la eficacia de su administración.
Además de la incertidumbre y el alto costo (el precio inicial era de 56 mil dólares por año), arrastraba los mismos efectos secundarios que las dos drogas actualmente aprobadas por la FDA: inflamación o hemorragia cerebral. Un asesor de ese organismo llegó a calificar la autorización del polémico Aduhelm como quizá “la peor decisión de aprobación que haya tomado la FDA que yo recuerde”.
Clarín, con información de AP y The New York Times